「〝藥〞走到哪? 還〝藥〞等多久?」記者會

癌友如王寶釧苦守寒窯 癡等不知盡頭 三大病團共同呼籲健保審核時程應透明、可追蹤 掌握卡關處對症下藥
癌症希望基金會與臺灣病友聯盟、罕見疾病基金會呼籲,新藥審查時程應「公開透明、可被追蹤監督」,才能讓各界了解目前新藥審查的進度。以民眾電商寄貨或訂餐為例,可從訂購開始追蹤送貨進度,直到完成寄件(如下圖),假如一個幾百元的商品都可以追蹤,一個動輒數千萬、甚至上億元的新藥案件更應要讓全民監督進度。因此,三個病團共同提出健保審議時程「透明化、可被追蹤」兩項訴求。

自2020年一路陪伴肺癌四期母親抗癌的陳小姐,等待新藥的過程深有所「痛」!陳媽媽因治療肺癌的標靶藥還沒有納入健保,不得已只能咬牙自費,年燒百萬的高昂費用讓家庭苦苦支撐。當陳小姐2022年發現這支藥品被放到新藥意見平台上,代表可能已進入健保審議程序,讓飽受沉重自費壓力的一家人終見一絲曙光,然而迄今近兩年,這支早已在健保審議中的藥品對病人而言還是「只聞樓梯響,不見藥到哪」!
等待期無規則可循 癌友家庭等到身心俱疲
健保署曾對外公布癌症新藥審查平均時間為13.7個月(約411天),和信醫院藥劑科主任陳昭姿的統計平均783天(約26.1個月),癌症希望基金會統計了自2016年迄今在健保署「新藥及新醫材病友意見分享平台」蒐集病人意見的癌症藥品或適應症,4成超過480天(約16個月)生效(正式納入健保給付)。不論是陳昭姿主任或癌症希望基金會提供的數據,兩者都與健保署對外公告之審查時間有明顯落差。
時程透明可追蹤 給病人一個看得見的盡頭
根據臺灣病友聯盟在2023年10月底針對聯盟團體調查資料顯示,16個病友團體中有9個病友團體認為,健保新藥等待的時間太長,且16個病友團體更全都表示「健保審查的流程不透明、難以掌握進度」, 罕見疾病基金會執行長陳冠如也指出,在11月初甫發布的罕病創新治療及藥物給付建言書中即已訴求「基於政府當責及公開透明,罕病新藥自申請到給付生效應公布各階段明確時程。」
食藥署能 健保署能不能?對症下藥才有效
三大病團呼籲除了應當有公開透明的機制和規則,也應該開放給公眾追蹤審查進度,讓病人看得到等待的盡頭,也讓各界對健保審查制度更有信心:
1. 時程公開透明 : 以食品藥物管理署(TFDA)為例,其設有規範清楚的藥品查驗登記審查時程,清楚標示藥廠送件後多久會討論、通知補件、完成審查、核發藥證等(如附件圖二),讓各界有規則可循。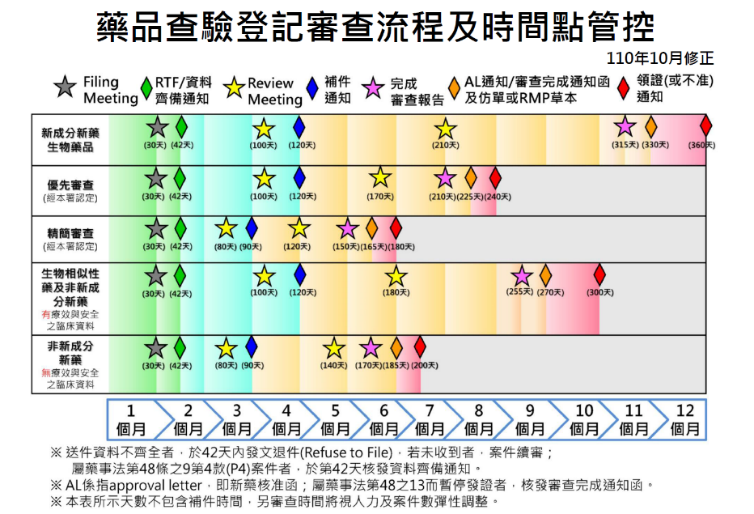
審查制度的透明化與可追蹤性,才能了解審查進度及卡關原因,以利對症下藥,也才能檢視新政策是否有效;若是因為新藥預算不足造成卡關,則應讓社會大眾知道,來年編列預算更應該編列充足,才能解決審查緩慢、病人等成「王寶釧」的現象。
